Determination of Three Benzalkonium Chloride Homologues in Environmental Water by Ultra High Performance Liquid Chromatography- Quadrupole/Electrostatic Field Orbitrap High Resolution Mass Spectrometry
-
摘要:
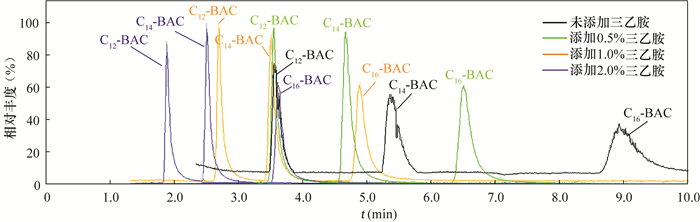
苯扎氯铵具有非氧化性杀菌作用,被大量应用于医疗卫生系统,随着污水排放到环境中,已被确定为可能严重影响生态系统中敏感生物的有害化合物,准确检测环境水体中苯扎氯铵的含量对于维护人体和生态环境健康具有重要意义。由于环境水体中残留苯扎氯铵的浓度低,且检测时容易受到复杂污染组分的干扰,结果出现假阳性,因此要求检测方法具有更低的检出限和更准确的定性能力。本文利用超高效液相色谱-四极杆-静电场轨道阱高分辨质谱技术(UPLC-Q-Orbitrap HRMS),建立了准确定性定量检测环境水体中苯扎氯铵三种同系物(十二烷基二甲基苄基氯化铵、十四烷基二甲基苄基氯化铵、十六烷基二甲基苄基氯化铵)的方法。样品经0.22μm孔径滤膜过滤,加入同等体积的甲醇混匀,流动相为含1%(V/V)三乙胺的10mmol/L乙酸铵-水溶液和甲醇,梯度洗脱,采用Accucore C18色谱柱(150mm×2.1mm,2.6μm)进行分离,6min内三种苯扎氯铵同系物实现基线分离,静电场轨道离子阱质谱在60000分辨率条件下以SIM模式进行数据采集。结果表明:三种苯扎氯铵在0.10~10.0μg/L浓度范围内线性关系良好(R>0.999),检出限为0.03~0.06μg/L,加标回收率为86.7%~111.2%。经实际样品验证,该方法在检出限和抗干扰能力上能够满足地表水和浅层地下水等环境水体中三种苯扎氯胺同系物的检测,并识别出十六烷基二甲基苄基氯化铵的疑似干扰物为质量数m/z 360.323的丙二醇脂肪酸酯。
-
关键词:
- 环境水体 /
- 苯扎氯铵 /
- 超高效液相色谱 /
- 四极杆-静电场轨道阱高分辨质谱法 /
- SIM模式
Abstract:BACKGROUND Benzalkonium chloride has a non-oxidizing bactericidal effect and is widely used in medical and health service. With the discharge of sewage into the environment, benzalkonium chloride has been identified as a harmful compound that may seriously inspect susceptible organisms in the ecosystem. Exact quantitative analysis of benzalkonium chloride in environmental water is of great significance for human and ecological environmental health. However, low content of benzalkonium chloride exist in environmental water. The interference of a complex matrix causes false positive results to occur easily. Therefore, the detection method is required to have lower detection limits and more accurate qualitative analysis ability.
OBJECTIVES To establish a method for the determination of three benzalkonium chloride homologues (n-C12H25-C9H13NCl, n-C14H29-C9H13NCl, n-C16H33-C9H13NCl) in environmental water.
METHODS Ultra-high performance liquid chromatography quadrupole/electrostatic field orbitrap high resolution mass spectrometry (UPLC-Q-Orbitrap HRMS) was used. The sample was filtered through a 0.22μm membrane, and then mixed with the same volume of methanol. The mobile phase consisted of 10mmol/L ammonium acetate aqueous solution which contained 1% (V/V) triethylamine as mobile phase B and methanol as phase A, with gradient elution. Accucore C18 column (150mm×2.1mm, 2.6μm) was used to separate the baseline of three benzalkonium chloride within 6 minutes, and the data were collected by electrostatic field orbitrap mass spectrometry in SIM mode at 60, 000 resolution.
RESULTS The contents of three benzalkonium chloride within the range of 0.10-10.0μg/L had a linear relationship (r>0.999). The detection limits ranged from 0.03 to 0.06μg/L. The recoveries of three kinds of benzalkonium chloride were 86.7%-111.2%.
CONCLUSIONS Verified by samples, this method meets the detection limits and has anti-interference abilities of three benzalkonium chloride homologues in surface water and shallow groundwater. Moreover, it was identified that the suspected disrupting chemical of cetyl dimethyl benzyl ammonium chloride is propylene glycol fatty acid ester at m/z 360.323.
-
-
表 1 苯扎氯铵同系物的母离子、产物离子及其强度
Table 1. Parent ions, product ions of benzalkonium chloride homologues and their response intensity
苯扎氯铵同系物 母离子 产物离子 质量数(m/z) 响应强度 质量数(m/z) 响应强度 C12-BAC 304.2988 4.10×107 91.0537(定量)
212.2354(定性)9.89×105
-C14-BAC 332.3300 4.56×107 91.0536(定量)
240.2673(定性)7.10×105
-C16-BAC 360.3613 3.27×107 91.0537(定量)
268.2991(定性)3.48×105
-表 2 三种苯扎氯铵同系物的方法特性指标
Table 2. Linear regression equations, correlation coefficients and detection limits of three benzalkonium chloride homologues
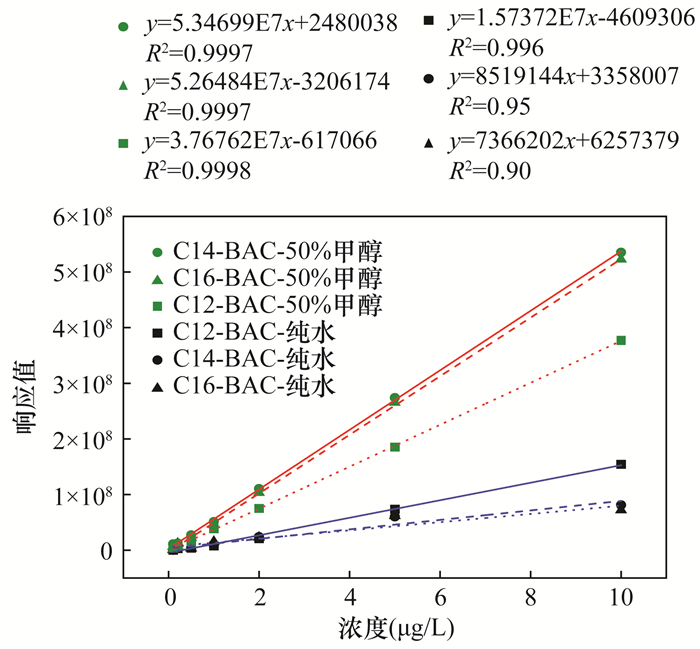
苯扎氯铵同系物 线性方程 线性范围(μg/L) 相关系数 检出限(μg/L) C12-BAC y=1.12×106+3.77×107x 0.10~10.0 0.9998 0.03 C14-BAC y=2.48×106+5.35×107x 0.10~10.0 0.9998 0.03 C16-BAC y=-3.21×106+5.26×107x 0.10~10.0 0.9998 0.06 表 3 三种苯扎氯铵同系物的加标回收率和精密度(n=6)
Table 3. Recoveries and RSD for three benzalkonium chloride homologues in spiked samples (n=6)
水样 苯扎氯铵同系物 加标量0.20μg/L 加标量1.00μg/L 加标量5.00μg/L 平均加标回收率(%) RSD (%) 平均加标回收率(%) RSD (%) 平均加标回收率(%) RSD (%) C12-BAC - - 94.2 5.5 92.3 3.9 地表水 C14-BAC - - 92.5 5.9 89.7 6.4 C16-BAC - - 90.7 7.7 89.6 5.6 C12-BAC 99.7 4.1 111.2 3.7 86.7 9.3 地下水 C14-BAC 88.6 6.5 91.2 4.2 89.3 7.1 C16-BAC 103.0 7.0 101.3 6.7 96.5 10.2 -
[1] Lavorgna M, Russo C, Dabrosca B, et al. Toxicity and genotoxicity of the quaternary ammonium compound benzalkonium chloride (BAC) using Daphnia magna and Ceriodaphnia dubia as model systems[J]. Environmental Pollution, 2016, 210: 34-39. doi: 10.1016/j.envpol.2015.11.042
[2] 张志芳, 谢立科, 孟祥慈, 等. 逍生散对干眼角膜上皮细胞损伤模型的干预研究[J]. 环球中医药, 2018, 11(3): 358-364. doi: 10.3969/j.issn.1674-1749.2018.03.009
Zhang Z F, Xie L K, Meng X C, et al. Intervention study of Xiaosheng powder on dry eye corneal epithelial cell injury model[J]. Global Traditional Chinese Medicine, 2018, 11(3): 358-364. doi: 10.3969/j.issn.1674-1749.2018.03.009
[3] 陈宇, 马贤德, 刘昱麟, 等. 山茱萸对苯扎氯铵诱导的干眼症小鼠视黄醇转运的调控作用[J]. 吉林大学学报(医学版), 2019, 45(4): 752-758. doi: 10.13481/j.1671-587x.20190402
Chen Y, Ma X D, Liu Y L, et al. Regulatory effects of fructus corni on retinol transport in mice with dry eye syndrome induced by benzalkonium chloride[J]. Journal of Jilin University (Medicine Edition), 2019, 45(4): 752-758. doi: 10.13481/j.1671-587x.20190402
[4] 安鸿雪, 任建姣, 马骏, 等. 苯扎氯铵对活性污泥微生物活性的影响[J]. 环境工程学报, 2020, 14(10): 2701-2709. doi: 10.12030/j.cjee.201911091
An H X, Ren J J, Ma J, et al. Effect of benzalkonium chloride on microbial activity of activated sludge[J]. Chinese Journal of Environmental Engineering, 2020, 14(10): 2701-2709. doi: 10.12030/j.cjee.201911091
[5] Kovacs-Hadady K, Fabian I. The determination of benzalkonium chloride in eye-drops by difference spectrophotometry[J]. Journal of Pharmaceutical and Biomedical Analysis, 1998(16): 733-740.
[6] Ma W X, Ma X D, Sha O, et al. Two spectrophotometric methods for the assay of benzalkonium chloride in bandage samples[J]. Journal of Surfactants and Detergents, 2014, 17: 177-181. doi: 10.1007/s11743-013-1446-4
[7] 李银华, 许钟元, 王振, 等. 铝试剂共振光谱散射光谱法测定苯扎氯铵含量的研究[J]. 精细石油化工, 2022, 39(2): 64-68. https://www.cnki.com.cn/Article/CJFDTOTAL-JXSY202202014.htm
Li Y H, Xu Z Y, Wang Z, et al. Study on determination of benzalkonium chloride by resonance lights scattering spectrometry with aluminon[J]. Speciality Petrochemicals, 2022, 39(2): 64-68. https://www.cnki.com.cn/Article/CJFDTOTAL-JXSY202202014.htm
[8] 李银华, 许钟元, 王振, 等. 共振光散射光谱法测定邦迪中苯扎氯铵含量[J]. 江苏海洋大学学报(自然科学版), 2020, 29(1): 71-74. https://www.cnki.com.cn/Article/CJFDTOTAL-HHGB202001014.htm
Li Y H, Xu Z Y, Wang Z, et al. Determination of benzalkonium chloride in bandage by resonance light scattering[J]. Journal of Jiangsu Ocean University (Natural Science Edition), 2020, 29(1): 71-74. https://www.cnki.com.cn/Article/CJFDTOTAL-HHGB202001014.htm
[9] Ly N H, Nguyen P D, Son S J, et al. Detection of benzalkonium chloride on glass surfaces using silver nanoparticles[J]. Bulletin of the Korean Chemical Society, 2022, 43: 246-254. doi: 10.1002/bkcs.12441
[10] Asghari A, Adl A, Ghajarbeygi P, et al. Rapid determination of benzalkonium chloride in aqueous samples by FTIR spectroscopy in tandem with chemometrics[J]. Infrared Physics and Technology, 2021, 116: 103762. doi: 10.1016/j.infrared.2021.103762
[11] 王萍, 李梦琦, 赵丽媛, 等. 基于均匀和正交试验设计的胶束电动毛细管色谱法同时测定消毒剂和抗抑菌产品中3种核苷类抗病毒药物[J]. 色谱, 2018, 36(9): 931-937. https://www.cnki.com.cn/Article/CJFDTOTAL-SPZZ201809015.htm
Wang P, Li M Q, Zhao L Y, et al. Uniform and orthogonal designs on experimental design and optimization of micellar electrokinetic capillary chromatographic method for the simultaneous analysis of three nucleoside antivirus drugs in disinfectant and anti/bacteriostatic products[J]. Chinese Journal of Chromatography, 2018, 36(9): 931-937. https://www.cnki.com.cn/Article/CJFDTOTAL-SPZZ201809015.htm
[12] 沈婵, 毛志平, 赵海浪, 等. 苯扎氯铵的快速检测方法及其在纺织工业中的应用[J]. 纺织检测与标准, 2022(1): 11-14. doi: 10.19391/j.cnki.cn31-2117.2022.01.016
Shen C, Mao Z P, Zhao H L, et al. Rapid detection method of benzalkonium chloride and its application in the textile industry[J]. Texile Tesing and Standard, 2022(1): 11-14. doi: 10.19391/j.cnki.cn31-2117.2022.01.016
[13] Lay-Keow N G, Hupe M, Harris A. Direct gas chroma-tographic method for determining the homologue composition of benzalkonium chlorides[J]. Journal of Chromatography, 1986, 351: 554-559. doi: 10.1016/S0021-9673(01)83537-8
[14] 黄博能. 气相色谱-质谱联用测定婴幼儿湿巾中苯扎氯铵的含量[J]. 中国纤检, 2015(20): 79-81. doi: 10.3969/j.issn.1671-4466.2015.20.027
Huang B N. Determination of benzalkonium chlorite in baby wipes by gas chromatography-mass spectrometry[J]. China Fiber Inspection, 2015(20): 79-81. doi: 10.3969/j.issn.1671-4466.2015.20.027
[15] 刘雯雯, 张瑾, 乔俊琴, 等. 复方化学消毒剂中苯扎氯铵的高效液相色谱测定[J]. 岩矿测试, 2011, 30(6): 677-682. doi: 10.3969/j.issn.0254-5357.2011.06.005
Liu W W, Zhang J, Qiao J Q, et al. Determination of benzalkonium chloride homologs in complex chemical disinfectant by high-performance liquid chromatography[J]. Rock and Mineral Analysis, 2011, 30(6): 677-682. doi: 10.3969/j.issn.0254-5357.2011.06.005
[16] Hashem A, Yasmin A. Determination of benzalkonium chloride in ophthalmic solutions by stability-indicating HPLC method: Application to a stability study[J]. Journal of Applied Pharmaceutical Science, 2016, 6(5): 80-89.
[17] 杨向妮, 姚志湘, 栗晖, 等. 斜投影和空间夹角判据结合紫外光谱分析滴眼液中苯扎氯铵[J]. 分析测试学报, 2016, 35(3): 337-341. doi: 10.3969/j.issn.1004-4957.2016.03.014
Yang X N, Yao Z X, Li H, et al. Rapid determination of benzalkonium chloride in eye drops with ultraviolet spectrum based on oblique projection and space angle criterion[J]. Journal of Instrumental Analysis, 2016, 35(3): 337-341. doi: 10.3969/j.issn.1004-4957.2016.03.014
[18] 杨龙华, 宿洁, 陈涛, 等. 高效液相色谱法测定复方混悬滴眼液中苯扎氯铵含量[J]. 中国药业, 2016, 25(2): 70-72. https://www.cnki.com.cn/Article/CJFDTOTAL-YYGZ201602027.htm
Yang L H, Su J, Chen T, et al. Determination of benzalkonium chloride in loteprednol and tobramycin ophthalmic suspension by HPLC[J]. China Pharmaceuticals, 2016, 25(2): 70-72. https://www.cnki.com.cn/Article/CJFDTOTAL-YYGZ201602027.htm
[19] 顾晓红, 顾炳仁, 蒋玲俐. 高效液相色谱法测定新霉素地塞米松滴眼液中苯扎氯铵的含量[J]. 安徽医药, 2017, 21(8): 1391-1394. doi: 10.3969/j.issn.1009-6469.2017.08.008
Gu X H, Gu B R, Jiang L L. The determination of benzalkonium chloride in neomycin dexamethasone eye drops by HPLC[J]. Anhui Medical and Pharmaceutical Journal, 2017, 21(8): 1391-1394. doi: 10.3969/j.issn.1009-6469.2017.08.008
[20] 张勇, 余权. 高效液相色谱法测定包装材料中苯扎氯铵含量[J]. 包装工程, 2017, 38(11): 60-63. https://www.cnki.com.cn/Article/CJFDTOTAL-BZGC201711015.htm
Zhang Y, Yu Q. Determination of benzalkonium chloride in packaging materials by high performance liquid chromatography[J]. Packaging Engineering, 2017, 38(11): 60-63. https://www.cnki.com.cn/Article/CJFDTOTAL-BZGC201711015.htm
[21] 成霈, 王妍, 郭松年. 超高效液相色谱法测定湿巾中的苯扎氯铵含量[J]. 当代化工研究, 2017(1): 35-36. https://www.cnki.com.cn/Article/CJFDTOTAL-ZJTY201701018.htm
Cheng P, Wang Y, Guo S N. Measurement of benzal-konium chloride content in moist wipes by super-efficient liquid chromatography method[J]. Modern Chemical Research, 2017(1): 35-36. https://www.cnki.com.cn/Article/CJFDTOTAL-ZJTY201701018.htm
[22] 周朝东, 黄哲甦. 高效液相色谱法测定鲑鱼降钙素鼻喷剂中苯扎氯铵的含量[J]. 天津药学, 2018, 30(5): 1-3. https://www.cnki.com.cn/Article/CJFDTOTAL-TJYA201805001.htm
Zhou C D, Huang Z S. Determination of benzalkonium chloride in salmon calcitonin nasal spray by HPLC[J]. Tianjin Pharmacy, 2018, 30(5): 1-3. https://www.cnki.com.cn/Article/CJFDTOTAL-TJYA201805001.htm
[23] Kostic D A, Mitic S S, Naskovic D C, et al. Determination of benzalkonium chloride in nasal drops by high-performance liquid chromatography[J]. E-Journal of Chemistry, 2012, 9(3): 1599-1604.
[24] Kulkarni P N, Dodake-Supekar A M, Gill C H. Simul-taneous determination of mometasone furoate and benzalkonium chlodide a stability indicating method[J]. Rasayan Journal Chemical, 2020, 13(3): 1522-1530.
[25] 郑国灿, 徐亚龙, 董浩然, 等. 高效液相色谱法测定牙膏中3种苯扎氯铵同系物[J]. 理化检验(化学分册), 2020, 56(10): 1102-1106. https://www.cnki.com.cn/Article/CJFDTOTAL-LHJH202010011.htm
Zheng G C, Xu Y L, Dong H R, et al. HPLC determination of 3 homologues of benzalkonium chloride in toothpaste[J]. Physical Testing and Chemical Analysis (Part B: Chemical Analysis), 2020, 56(10): 1102-1106. https://www.cnki.com.cn/Article/CJFDTOTAL-LHJH202010011.htm
[26] 陈小轲, 沈婵, 曹石淼, 等. 高效液相色谱法测定纺织品中3种苯扎氯铵同系物[J]. 印染, 2021(12): 53-56. https://www.cnki.com.cn/Article/CJFDTOTAL-YIRA202112013.htm
Chen X K, Shen C, Cao S M, et al. Determination of 3 benzalkonium chloride homologs in textiles by high performance liquid chromatography[J]. China Dyeing & Finishing, 2021(12): 53-56. https://www.cnki.com.cn/Article/CJFDTOTAL-YIRA202112013.htm
[27] 孙龙, 邵明媛, 王浩. LC/MS/MS测定婴幼儿配方乳粉中3种苯扎氯铵同系物[J]. 食品研究与开发, 2017, 38(1): 165-169. https://www.cnki.com.cn/Article/CJFDTOTAL-SPYK201701044.htm
Sun L, Shao M Y, Wang H. Simultaneous determination of three kinds of benzalkonium chloride homologs in infant formula milk powder by LC/MS/MS[J]. Food Research and Development, 2017, 38(1): 165-169. https://www.cnki.com.cn/Article/CJFDTOTAL-SPYK201701044.htm
[28] 王浩, 陈江龙, 张杉, 等. 液相色谱-串联质谱法测定婴幼儿配方乳粉中六种消毒剂残留[J]. 中国乳品工业, 2019, 47(1): 46-48. https://www.cnki.com.cn/Article/CJFDTOTAL-RPGY201901011.htm
Wang H, Chen J L, Zhang S, et al. Determination of six disinfectants in infant milk powder by high performance liquid chromatography-tandem mass spectrometry[J]. Dairy Industry, 2019, 47(1): 46-48. https://www.cnki.com.cn/Article/CJFDTOTAL-RPGY201901011.htm
[29] 查越, 沈学静, 李明. 基于纳升电喷雾-便携式离子阱质谱的苯扎氯铵快检方法[J]. 分析试验室, 2021, 40(10): 1166-1170. https://www.cnki.com.cn/Article/CJFDTOTAL-FXSY202110007.htm
Zha Y, Shen X J, Li M. Fast detection of benzalkonium chloride in eye drops based on nano electrospray-portable ion trap mass spectrometry[J]. Chinese Journal of Analysis Laboratory, 2021, 40(10): 1166-1170. https://www.cnki.com.cn/Article/CJFDTOTAL-FXSY202110007.htm
[30] 沈婵, 毛志平, 赵海浪, 等. 基于HPLC-MS/MS技术测定纺织品中的苯扎氯铵[J]. 印染, 2022(2): 68-72. https://www.cnki.com.cn/Article/CJFDTOTAL-YIRA202202015.htm
Shen C, Mao Z P, Zhao H L, et al. Determination of benzalkonium chloride in textiles by HPLC-MS/MS[J]. China Dyeing & Finishing, 2022(2): 68-72. https://www.cnki.com.cn/Article/CJFDTOTAL-YIRA202202015.htm
[31] Kang H I, Shin H S. Rapid and sensitive determination of benzalkonium chloride biocide residues in soil using liquid chromatography-tandem mass spectrometry after ultrasonically assisted extraction[J]. Bulletin of the Korean Chemical Society, 2016, 37: 1219-1227.
[32] Kim T K, Jang M, Hwang Y S, et al. Adsorption of benzalkonium chlorides onto polyethylene microplastics: Mechanism and toxicity evaluation[J]. Journal of Hazardous Materials, 2022, 426: 128076.
[33] 杨芬, 谢邵文, 韦朝阳, 等. HPLC-ICP-MS联用技术研究甲醇对砷形态分析结果的影响[J]. 光谱学与光谱分析, 2018, 38(6): 1884-1888. https://www.cnki.com.cn/Article/CJFDTOTAL-GUAN201806047.htm
Yang F, Xie S W, Wei C Y, et al. Effects of methanol addition on arsenic speciation analysis with HPLC-ICP-MS[J]. Spectroscopy and Spectral Analysis, 2018, 38(6): 1884-1888. https://www.cnki.com.cn/Article/CJFDTOTAL-GUAN201806047.htm
[34] 宋淑玲, 郭晓辰, 胡小建, 等. 气相色谱-高分辨质谱联用测定地下水中16种典型痕量含氯持久性有机污染物[J]. 岩矿测试, 2013, 32(2): 319-324. doi: 10.3969/j.issn.0254-5357.2013.02.022
Song S L, Guo X C, Hu X J, et al. Determination of 16 typical chlorinated persistent organic pollutants in groundwater by gas chromatography-high resolution mass spectrometry[J]. Rock and Mineral Analysis, 2013, 32(2): 319-324. doi: 10.3969/j.issn.0254-5357.2013.02.022
-


 下载:
下载: